Современные технологии позволяют проводить оплодотворение и выращивать эмбрионы на ранних стадиях развития вне тела человека.
Методы оплодотворения
Все зрелые яйцеклетки, полученные в результате протокола ЭКО, подлежат оплодотворению.
Классическое ЭКО подразумевает минимальное вмешательство эмбриолога в этот процесс. Яйцеклетки и специально обработанные сперматозоиды помещаются в питательную среду, где они взаимодействуют так же, как в организме женщины. Такой метод оплодотворения подойдет парам с хорошим качеством эякулята и достаточным количеством яйцеклеток.
В более сложных случаях, например, при плохом качестве эякулята (то есть если сперматозоидов мало, снижена их подвижность или много аномальных сперматозоидов), предпочтение отдается другой методике оплодотворения – ИКСИ (от английского ICSI – Intra Cytoplasmic Sperm Injection, интроцитоплазматическая инъекция сперматозоида). Если говорить простым языком, методика ИКСИ позволяет ввести сперматозоид непосредственно внутрь яйцеклетки. ИКСИ применяется также, если в предыдущих попытках ЭКО не наступило оплодотворение или был зафиксирован низкий процент оплодотворенных яйцеклеток. Бывают такие нарушения, при которых сперматозоид «не замечает» яйцеклетку или не может проникнуть через ее оболочку, чтобы оплодотворить.
Существует также еще более усовершенствованная методика – ИМСИ (Intra Сytoplasmic morphologically selected sperm injection, инъекция морфологически отобранного сперматозоида). Это вариация ИКСИ, при которой выбор сперматозоида для оплодотворения выполняется под специально оборудованным микроскопом. Очень большое цифровое увеличение позволяет рассмотреть не только внешние, но и внутренние дефекты в клетке и отобрать самые морфологически правильные сперматозоиды. Чаще всего ИМСИ рекомендуется паре после нескольких неудачных попыток ИКСИ или при большом количестве патологических форм сперматозоидов в эякуляте.
Разумеется, применение этих технологий всегда оговаривается с пациентами, поскольку требует дополнительных затрат. Врач и эмбриолог изучают анамнез пары, историю предыдущих попыток ЭКО, качество полученных клеток и потом могут предложить применение дополнительных методов.
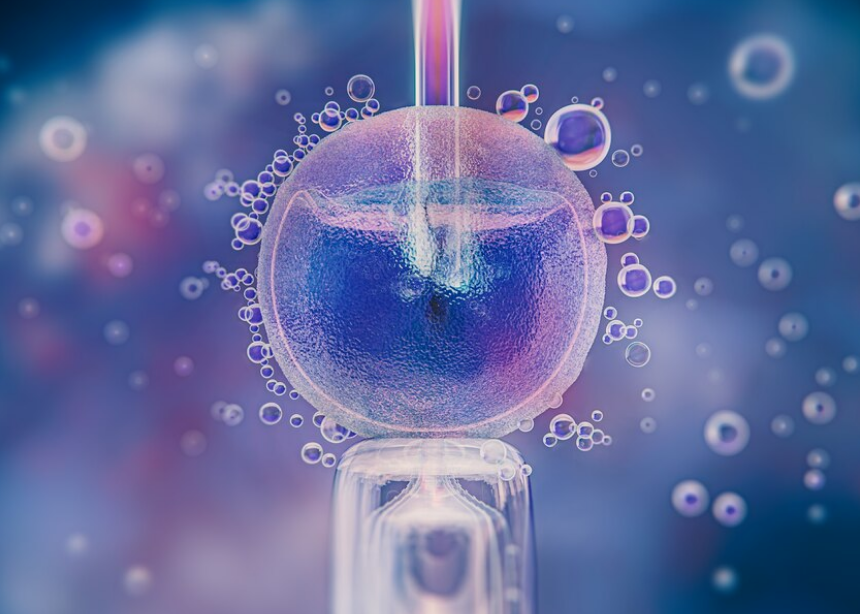
Стадии развития эмбриона
В эмбриологических протоколах день пункции и оплодотворения обозначается как день 0.
Дальнейшее развитие эмбрионов проходит одинаково, независимо от метода оплодотворения. Длительность культивирования может составлять от 2 до 5 (реже 6) дней. Эмбриолог ежедневно наблюдает за делением клеток и вносит данные в протокол культивирования.
Утром следующего дня (день 1) необходимо оценить оплодотворение каждой яйцеклетки под микроскопом. Если яйцеклетка оплодотворилась правильно, мы увидим в ней 2 пронуклеуса: один отцовский и один материнский (это структуры, которые несут хромосомы от каждого из родителей, при их слиянии формируется ядро с хромосомным набором нового человека). Клетки без признаков оплодотворения, а также с аномальным оплодотворением (с одним пронуклеусом, тремя и более) необходимо удалить. Эти зиготы (клетки, образующиеся в результате оплодотворения) несут аномальный набор хромосом, но сохраняют способность к делению (причем на этапе деления такой эмбрион уже невозможно будет отличить от нормального по внешним признакам). Применение технологий ИКСИ и ИМСИ позволяет уменьшить случаи аномального оплодотворения, но, к сожалению, не может полностью исключить их.
День 2. Эмбрион должен иметь от 2-х до 4-х бластомеров (клетки, образующиеся в результате деления зиготы). В идеале бластомеры должны быть ровными, равными по размеру, округлыми.
День 3. Идеальный эмбрион должен иметь уже 8 бластомеров. Оценивается не только форма бластомеров, но и их расположение относительно друг друга.
День 4 – морула (завершающая стадия деления зиготы). Все клетки сливаются и начинают объединяться в группы, которые далее будут формировать внешние и внутренние клеточные массы.
День 5 – бластоциста (ранняя стадия развития зародыша). На этой стадии эмбрионы могут довольно сильно отличаться друг от друга, что и позволяет нам выбрать лучших для переноса в полость матки. Чаще всего на пятый день бластоциста выходит из оболочки, которая окружала ее все это время. Теперь эмбрион готов имплантироваться (прикрепиться) в матку и дальнейшее культивирование в инкубаторе невозможно.
Перенос эмбриона в матку может выполняться в любой день развития. Однако здесь все очень индивидуально. Если у пациентов много эмбрионов, то дальнейшее культивирование помогает нам выбрать одного-двух наиболее перспективных (которые росли лучше всех), чтобы повысить шансы на наступление беременности. Но если у пациентов в результате оплодотворения получились всего один или два эмбриона – выбирать не из чего, и можно уже во второй день выполнять перенос в матку, где эмбрионам будет лучше, чем в любом инкубаторе.
К сожалению, бывает и так, что переносить нечего. На любом этапе ЭКО могут возникнуть сложности: не получены яйцеклетки, не произошло оплодотворение, замерли в развитии эмбрионы и т.д. В таком случае женщина снимается с протокола и после перерыва может начинать готовиться к следующему.
Разумеется, мы стараемся переносить самые лучшие эмбрионы, но предсказать дальнейшее их «поведение» сложно. Эмбрионы самого хорошего качества не гарантируют наступления беременности, и, наоборот, из откровенно «некрасивых» эмбрионов рождаются прекрасные дети. Морфологический отбор (по внешним признакам) никак не исключает генные и хромосомные аномалии.
Здесь хочется сказать, что риски родить ребенка с пороками развития и врожденными аномалиями после ЭКО точно такие же, как и при естественной беременности. В этом играют роль лишь определенные наборы хромосом и механизмы их взаимодействия, но никак не способ оплодотворения.
Предимплантационная генетическая диагностика
Исключить риски врожденных пороков и генетических аномалий по морфологическим признакам (внешнему виду, размеру, строению сперматозоида, яйцеклетки или эмбриона) невозможно, как и определить пол будущего ребенка. Связь между морфологией и генетикой довольно поверхностна. Разумеется, более вероятно, что сперматозоид или эмбрион с видимыми дефектами строения может иметь и хромосомные аномалии. В то же время нормальные (с точки зрения морфологии) клетки также могут нести генетические отклонения. Предугадать это, к сожалению, невозможно, точно так же, как и при естественной беременности. Здесь могут сработать методы отбора самого организма – имплантация и вынашивание. Очень часто самопроизвольные выкидыши и замершие беременности на самых разных сроках говорят нам именно о том, что плод был с серьезными генетическими патологиями или отклонениями, которые не совместимы с жизнью. Если же такой механизм отбора дает сбой, рождается ребенок с пороками развития.
Исключить определенные генные и хромосомные аномалии помогает предимплантационная генетическая диагностика эмбрионов.
Эта процедура подразумевает исследования хромосомного и генного набора эмбриона с целью исключения конкретных аномалий и (при необходимости) определения пола будущего малыша (чтобы исключить заболевания, поражающие только ребенка определенного пола). Существуют различные методики и подходы к проведению таких исследований. Все чаще предимплантационная генетическая диагностика выполняется на стадии бластоцисты (на 5-й день развития эмбриона). Структура бластоцисты такова, что она содержит часть клеток, из которых будет развиваться сам эмбрион, и часть, которая будет формировать плаценту и оболочки (часть именно этих клеток можно безболезненно для эмбриона «отнять» для проведения диагностики). Полученные клетки подвергаются исследованиям самыми разными методами, в зависимости от того, какие патологии и нарушения нужно исключить. Исследовать эмбрионы сразу на все невозможно, поскольку попросту не хватит материала, поэтому предимплантационная диагностика проводится прицельно. То есть исключаются только определенные патологии (к которым есть склонность или предрасположенность у родителей). Чаще проводятся скрининговые исследования для исключения самых распространенных числовых аномалий хромосом – трисомии по 21, 18, 13 хромосомам, отклонений в числе половых хромосом (синдром Клайнфельтера, синдром Тернера) и др. Традиционный «набор» включает исследование около 8 хромосом. Генных заболеваний намного больше, поэтому они исследуются по показаниям, то есть генетикам нужно знать, что искать. Но, опять же, предимплантационная диагностика не может на 100% гарантировать здорового ребенка. Мы исключаем лишь определенные аномалии и заболевания, но это не значит, что не может быть других.
Предимплантационная диагностика требует немало времени, поэтому, как правило, после биопсии эмбрионы подвергаются криоконсервации (замораживаются) и размораживаются для подсадки только после получения результатов всех исследований. Криоконсервация тоже несет в себе пусть небольшие, но риски, эмбриону нужно успешно пережить замораживании и размораживание. Разумеется, наука не стоит на месте, и специалисты постоянно совершенствуют методы этих исследований.
Криоконсервация
Мы не можем переносить больше двух эмбрионов (в некоторых случаях, оговоренных Законом о вспомогательных репродуктивных технологиях, больше трех), чтобы снизить риск многоплодной беременности, поскольку женщина должна выносить и родить здорового ребенка. Если у пары остались эмбрионы хорошего качества, их можно криоконсервировать (заморозить). Криоконсервация в жидком азоте при температуре -196°С позволяет остановить все обменные процессы в клетке так, чтобы она не жила, но и не умирала. Самая большая проблема криоконсервации – вода, которая находится вокруг клетки и внутри нее. При замерзании вода образует кристаллы льда, которые, как острые ножи, режут и рвут клетки и внутриклеточные структуры. Поэтому, чтобы обезопасить клетки, перед замораживанием эмбрион сначала проводится через ряд растворов криопротекторов (специальных веществ, которые замещают воду и не образуют острых кристаллов при низких температурах), напитывается этими веществами и потом консервируется в жидком азоте на специальных носителях.
Замораживать можно как эмбрионы на любой стадии развития, так и сперматозоиды и яйцеклетки. Храниться законсервированные клетки могут сколь угодно долго, и после размораживания они абсолютно ничем не отличаются от «свежих» эмбрионов и клеток. Однако определенные риски здесь все же присутствуют: эмбрион может погибнуть при замораживании или размораживании. Но, во-первых, современные методики дают до 98% выживаемости эмбрионов, а во-вторых, у эмбрионов очень хорошие восстановительные способности. Даже если при замораживании (размораживании) погибла часть клеток, это еще не означает, что погиб сам эмбрион.
Разумеется, услуга криоконсервации платная, отдельно оплачивается и хранение. Клетки хранятся в криососуде, в котором постоянно испаряется азот. На его закупку и требуются деньги.
Вспомогательный хэтчинг
Это процедура, которая помогает эмбриону «вылупиться» из своей блестящей оболочки (через нее же должен пробиться сперматозоид, чтобы оплодотворить яйцеклетку). Блестящая оболочка – это своего рода скорлупа, защищающая эмбрион, который внутри нее развивается до стадии бластоцисты. Если с оболочкой что-то не так (она очень эластичная или толстая), эмбрион попросту не сможет из нее «вылупиться» – соответственно, имплантироваться, и погибнет в этом яйце.
Вспомогательный хэтчинг может быть разным: лазерный, химический, механический. Но суть его одна – сделать «насечки» на оболочке эмбриона, которые помогут ему «вылупиться» и имплантироваться. Кроме того, хэтчинг является обязательным элементом предимплантационной диагностики. Без повреждения блестящей оболочки просто не получится взять необходимые клетки для диагностики.
Как видно, современная наука и медицина имеют довольно большой ресурс возможностей, чтобы помочь супругам стать родителями вопреки всему и несмотря ни на что. Пожалуй, к этому арсеналу остается добавить лишь веру. Твердую веру в друг друга, во врача, который вам помогает, ну и, конечно, в будущего малыша, который пусть и маленькими шагами, но уже двигается вам навстречу! Верьте, что она не за горами!
